Editor
ВАКЦИНА ПРОТИ ПНЕВМОКОКОВОЇ ІНФЕКЦІЇ
Група/призначення:
Вакцина полівалентна. Покази: профілактика пневмококових інфекцій, при введенні вакцини викликається продукція антитіл до капсулярних полісахаридів Streptococcus pneumoniae, забезпечуючи специфічний захист від інфекції.
Альтернативні назви / синоніми:
Пневмовакс-23 (23 типи Streptococcus pneumoniae) .
Діюча речовина:
Пневмококові кон’югати (Pneumococcus, purified polysaccharides antigen).
Рекомендації при вагітності: сумісна.
Рекомендації при лактації:
Відсутня інформація про застосування у людини; ймовірно сумісна.
Прийом під час вагітності (короткий висновок):
Ризик для плода при вакцинації в І триместрі невідомий. Однак, згідно з рекомендаціями американської колегії акушерів та гінекологів, покази до застосування цього типу вакцини не змінюються у зв’язку з вагітністю. Підвищені концентрації антитіл були виявлені у жінок через 1 рік після антенатальної імунізації. Консультативний комітет з практики імунізації США повідомляє про відсутність інформації щодо несприятливих наслідків у немовлят, матері яких були випадково вакциновані при вагітності.
Інформація щодо досліджень на тваринах: не проводились.
Інформація щодо впливу на плід:
Рев’ю 1991 року повідомляє, що материнські антитіла, індуковані вакциною, проникають до плаценти і забезпечують захист новонародженого.
Дослідження, які проводились в Бангладеш (1995 рік) повідомляють про введення протипневмококової вакцини здоровим жінкам у терміні 30-34 тижнів вагітності. Жінкам контрольної групи вводили протименінгококову вакцину. За імунною відповіддю немовлят в результаті імунізації матерів спостерігали від народження до 5 місяців життя. Продемонстровано, що до плода проникає достатня кількість специфічних імуноглобулінів G для забезпечення пасивного імунітету проти пневмококової інфекції. Автори дійшли висновку, що в регіонах, де пневмококова інфекція є серйозною проблемою охорони здоров’я, материнська імунізація є безпечним і недорогим способом зниження частоти інфекції, якщо наступні дослідження не продемонструють, що пасивна імунізація немовлят порушує активну імунізацію надалі протягом життя.
При дослідженні 1996 року пневмококову полівалентну вакцину призначали в ІІІ триместрі як спробу захистити дитину протягом перших місяців життя. Ступінь та тривалість захисту були непевними, оскільки пневмококові антитіла у немовлят швидко зникали.
Повідомлення 1998 року відзначає, що потрібно провести велике дослідження для з’ясування, чи материнська імунізація знижує смертність та захворюваність немовлят. Через високу вартість нових кон’югованих вакцин один з авторів вважає, що вакцинація вагітних полісахаридними вакцинами може бути найпрактичнішим методом попередження пневмококового сепсису у новонароджених в країнах, що розвиваються.
Застосування препарату під час вигодовування:
У вищенаведеному дослідженні, яке проводилось в Бангладеш, відзначали значне підвищення титру специфічного імуноглобуліну А (IgA) в молозиві матерів, які отримали полівалентну вакцину у терміні 30-34 тижнів вагітності. Титри антитіл залишались вищими до 5-ти місяців в порівнянні з контрольною групою.
Вплив на фертильність (чоловіків та жінок): відсутня інформація.
Адаптовано за матеріалами:
- Інформаційна система Центру репродуктивної токсикології “Reprotox” (http://www.reprotox.org).
- Briggs G, Freeman R, Yaffe S. Drugs in Pregnancy and Lactation: a Reference Guide to Fetal and Neonatal Risk. Ninth edition, 2011, Wolters Kluwer, Lippincott Williams & Wilkins. 1728 pages. ISBN: 978-1-60831-708-0.
Адаптовано 11.04.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних наук, доцент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Переглянуто редакційною колегією 26.04.2016 р.
ТРИМЕТОБЕНЗАМІД
Група/призначення: антиеметичний засіб.
Альтернативні назви / синоніми: не має.
Діюча речовина: триметобензамід.
Рекомендації при вагітності:
Дані про застосування у людини припускають низький ризик.
Рекомендації при лактації:
Відсутні дані про застосування у людини; ймовірно сумісний.
Прийом під час вагітності (короткий висновок):
Дані від експериментальних тварин та обмежені дані про використанні у людини не припускають значного зростання ризику вроджених вад.
Інформація щодо досліджень на тваринах:
Репродуктивні дослідження у щурів та кролів не продемонстрували тератогенності препарату. При дозах 20 та 100 мг/кг у щурів та 100 мг/кг у кролів спостерігали підвищену частоту резорбції плодів.
Інформація щодо впливу на плід:
Досвід застосування обмежений. Невідомо, чи триметобензамід проникає до плаценти, але молекулярна вага препарату це припускає.
Триметобензамід призначають при вагітності для лікування токсикозу без несприятливих наслідків.
В одному дослідженні 193 жінки отримували триметобензамід в І триместрі. Частота вроджених вад у віці 1 місяця, 1 року, 5 років становила – 2,6%, 2,6% та 5,8%, відповідно. Зростання частоти до 5,8% спостерігали при порівнянні з нелікованими контролями (3,2%). Автори відзначають також прийом інших препаратів вагітними і вважають, що триметобензамід не асоціюється з підвищеним ризиком вроджених вад розвитку.
Застосування препарату під час вигодовування:
Невідомо, чи триметобензамід проникає до грудного молока, але його молекулярна вага це припускає. Вплив препарату на немовля, яке знаходиться на грудному вигодовуванні, невідомий.
Вплив на фертильність (чоловіків та жінок): відсутня інформація.
Адаптовано за матеріалами:
- Briggs G, Freeman R, Yaffe S. Drugs in Pregnancy and Lactation: a Reference Guide to Fetal and Neonatal Risk. Ninth edition, 2011, Wolters Kluwer, Lippincott Williams & Wilkins. 1728 pages. ISBN: 978-1-60831-708-0
Адаптовано 30.03.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних нанук, доцент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Переглянуто редакційною колегією 26.04.2016 р.
ОНДАНСЕТРОН
Назва англійською мовою: ondansetron.
Група/призначення:
Антиеметичний засіб. Селективний антагоніст 5-НТ3 серотонінових рецепторів. Схвалений для лікування нудоти та блювоти, спричиненої хіміотерапією, радіотерапією, після хірургічного втручання. Також призначається вагітним з приводу токсикозу
Згідно статистики FDA за період 2001 – 2015 років антиеметики використовувались при 2,3 млн. вагітностях, з них в 15,2% це був ондансетрон. Найчастіше препарат застосовували в І триместрі вагітності. |
| ДАНІ ПРО АСОЦІЙОВАНІ З ОНДАСЕНТРОНОМ ВРОДЖЕНІ ВАДИ РОЗВИТКУ Є СУПЕРЕЧЛИВИМИ.
НАЙБІЛЬШ ЙМОВІРНІ АСОЦІАЦІЇ З РОЗЩІЛИНОЮ ПІДНЕБІННЯ ТА ВРОДЖЕНИМИ ВАДАМИ СЕРЦЯ |
| інші вади, які можливо асоціюються з ондансетроном: діафрагмальна кила, агенезія/дизгенезія нирок, аномалії вуха, аномалії органів дихання |
| НИЖЧА ЧАСТОТА СПОНТАННОГО ПЕРЕРИВАННЯ ВАГІТНОСТІ ТА БІЛЬША КІЛЬКІСТЬ НАРОДЖЕНИХ ЖИВИМИ ДІТЕЙ у жінок, які з приводу гіперемезис вагітних (hyperemesis gravidarum) отримували ондансентрон |
| ВАЖЛИВО: ЄДИНИМ СХВАЛЕНИМ FDA МЕДИКАМЕНТОМ ДЛЯ ЛІКУВАННЯ ТОКСИКОЗУ ВАГІТНИХ Є
ДОКСИЛАМІН-ПІРИДОКСИН |
| ТАКА КОМБІНАЦІЯ ВВАЖАЄТЬСЯ БЕЗПЕЧНОЮ ДЛЯ ПЛОДУ І ТОМУ РЕКОМЕНДОВАНА ТАКОЖ АМЕРИКАНСЬКОЮ КОЛЕГІЄЮ АКУШЕРІВ/ГІНЕКОЛОГІВ ЯК ПРЕПАРАТ ВИБОРУ ДЛЯ ВАГІТНИХ |
Також при призначенні ондансетрону рекомендовано проводити моніторинг серцевої діяльності вагітної (електрокардіографію).
Альтернативні назви / синоніми: зофран, zuplenz.
Діюча речовина: ондансетрон.
Рекомендації при вагітності:
Протипоказаний, принаймі, в І триместрі.
Рекомендації при лактації:
Відсутні дані про застосування у людини; ймовірно сумісний.
Прийом під час вагітності (короткий висновок):
Два великі національні дослідження (Данія та Швеція) виявили значне збільшення частоти серцевих аномалій при використанні ондансетрону в І триместрі. Також велике національне дослідження в США виявило підвищений ризик орофаціальних розщілин, але невроджених вад серця. Ондансетрон, зазвичай, призначається в період органогенезу, коли спостерігається пік проявів токсикозу вагітних. У випадку необхідності призначення ондансетрону для матері, слід уникати цього в І триместрі.
Інформація щодо досліджень на тваринах:
Репродуктивні дослідження у щурів та кролів з пероральними дозами, які у 6 разів та 24 рази перевищували максимальну рекомендовану дозу для людини відповідно не продемонстрували неспричтливого впливу на фертильність та розвиток плоду. Не виявлено карциногенності та мутагенності.
Інформація щодо впливу на плід:
РЕЗУЛЬТАТИ ТЕРАТОЛОГІЧНИХ ДОСЛІДЖЕНЬ:
Великі вроджені вади загалом: не виявлено асоціації з плікуванням матерів 3277 новонароджених ондансетроном у І триместрі (когортне дослідження на основі програми Medicaid (США). Аналогічні дані від шведського дослідження в групі 1349 немовлят, чиї матері отримали рецепт на ондансетрон на дуже ранніх термінах вагітності, 1233 – у І триместрі данського дослідження з вивчення бази рецептурних призначень, 211 – за даними австралійського, пов’язаного з рецептурними базами дослідження. 90% матерів 922 новонароджених лікували гіперемезис ондансетроном в І триместрі без істотного підвищення частоти вроджених вад в порівнянні з контрольною групою. Мета-аналіз доступних досліджень не продемонстрував підвищеного ризику вроджених вад.
Кардіоваскулярні аномалії: шведське дослідження повідомило про підвищення ризику (співвідношення шансів 1,62, 95% ДІ 1,04-2.54), особливо дефекти перетинок серця (відносний ризик 2,05, 95% ДІ 1,19-3,28) – серед 1349 немовлят, чиї мами отримали рецепт на ондансетрон на ранньому терміні вагітності. Аналіз випадок-контроль 303 дітей з вродженими вадами серця показав зв’язок з лікуванням матері ондансетроном в І триместрі (співвідношення шансів 1,43, 95% ДІ 1,28-1,61) – за рахунок дефекту міжшлуночкової перетинки (ДМШП) (1,29, 95% ДІ 1,03-1,61), дефекту міжпередсердної перегортинки (ДМПП) (1,49, 95% ДІ 1,32-1,69), атріовентрикулярного септального дефекту (2,71, 95% ДІ 1,62-4,52), інших (1,75, 95% ДІ 1,39-2,20). В той же час не було виявлено такої асоціації серед 1345 немовлят з ДМШП та 1205 з вторинним ДМПП в дослідженні з запобігання вродженим вадам розвитку (the National Birth Defects Prevention Study) та серед 1327 дітей з ДМШП і 364 з вторинним ДМПП в дослідженні the Slone Birth Defects Study. Не виявлено асоціації і в данському дослідженні з охопленням 1233 жінок, які лікувались в І триместрі.
Розщілна піднебіння: когортне дослідження від Medicaid США виявило вищу за очікувану частоту серед 88465 новонароджених, чиї мами отримували в І триместрі ондансетрон (відносний ризик 1,24, 95% ДІ 1,03-1,48, n=124). Аналогічна асоціація з розщілиною піднебіння отримана в двох дослідженнях від the National Birth Defects Prevention Study – 525 та 418 дітей – відносний ризик 2,4, 95% ДІ 1,2-4,8 та 1,6, 95% ДІ 1,1-2,3 відповідно. В той же час дослідження the Slone Birth Defects Study не знайшло такого зв’язку з ондансетроном серед 287 немовлят з розщілиною піднебіння, а також іншими проектами з охопленням 1590 та 1068 дітей з розщілинами піднебіння.
Інші вади розвитку: 1) діафрагмальна кила – вища за очікувану частота лікування ондансетроном в І триместрі матерів 464 дітей (співвідношення шансів 1,40, 95% ДІ 1,05-1,87), подібні дані в the National Birth Defects Prevention study (1,5, 95% cДІ 1,0-2,4). На противагу цим даним – жодного випадку діафрагмальної кили в групі 1349 та 1233 новонароджених з пренатальним впливом ондансетрону в ході датських та шведських досліджень; 2) агенезія/дизгенезія нирок у 159 немовлят – частіша за очікувану частота використання в І триместрі ондансетрону – the Slone Birth Defects Study (1,8, 95% ДІ 1,4-13,0), аналогічні дані від 8638 немовлят з аномаліями збиральної системи нирок (1,07, 95% ДІ 1,00-1,16) -від бази даних медичного страхування США; але рідко зустрічались ці аномалії серед 1349 або 1233 немовлят, які отримували ондансетрон, у шведських і датських дослідженнях; 3) аномалії вуха та органів дихання – (відносний ризик 1,67, 95% ДІ 1,17-2,37) та (відносний ризик=1,13, 95% ДІ 1,01-1,28) серед 88 446 немовлят, матері яких отримували ондансетрон за рецептом під час І триместру вагітності в когортному дослідженні Medicaid США; не виявлено такого зв’язку в шведському і датському дослідженнях.
Спонтанні аборти, мертвонародження, інші результати вагітностей: у жінок, які приймали ондансетрон з приводу гіперемезис гравідарум відмічено нижчу частоту самовільних переривань І триместру (співвідношення шансів 0,09, 95% ДІ 0,06-0,13) та більшу кількість ніроджених живими (3,59, 95% ДІ 2,91-4,44) в порівнянні з жінками з таким самим станом без лікування цим препаратом – згідно опитування ретроспективного когортного дослідження (2016). Подібні дані щодо самовільних абортів отримано і в ході проспективного когортного дослідження з охопленням жінок, які з приводу токсикозу приймали ондансетрон і звернулись в тератологічну службу (2017). Інші дослідження не виявили асоціації ондакнсетрону з самовільним перериванням, передчасним народженням, мертвонародженням, зниженням ваги новонароджених (2004, 2013, 2016).
Продемонстровано плацентарний трансфер ондансетрону в І триместрі.
Окремі випадки, пов’язані з використанням ондансетрону у вагітних:
Повідомляється про 21-річну першовагітну з важкими проявами токсикозу, яка безуспішно лікувалась протягом 4 тижнів, починаючи з 6 тижня наступними препаратами: метоклопрамідом 10 мг внутрішньовенно тричі на день (стимулятор перистальтики), дименгідринатом ректально 100 мг двічі на день та внутрішньовенно (антигістамінний препарат). Стан плода та матері було визнано загрозливим і, починаючи з 11 тижня, призначено ондансетрон внутрішньовенно 8 мг тричі на день на 14 днів. На другий день терапії спостерігали значне покращення стану вагітної. Жінка народила здорову дівчинку вагою 3,2 кг.
Інше повідомлення інформує про 22-річну вагітну з нефротичним синдромом. Лікування ондансетроном розпочали на 30 тижні – 8 мг внутрішньовенно тричі на день протягом одного дня, далі – перорально до 33 тижня (доза не зазначена). Народилась здорова дитина шляхом планового кесаревого розтину вагою 2,05 кг.
У 2004 році повідомили про випадок кишкової непрохідності у вагітної після прийому ондансетрону протягом 3 місяців при вагітності. Після припинення прийому препарату та зникнення непрохідності народилась здорова дитина у віці 41 тижня. Кишкова непрохідність вважається побічним ефектом ондансетрону також згідно з іншими повідомленнями.
У 2008 році повідомили про транзиторні екстрапірамідні порушення у недоношеного немовляти, чия мама приймала циталопрам та ондансетрон на пізніх термінах вагітності. Такий побічний ефект пояснюється впливом 2 препаратів.
Повідомляється про внутрішньовенне введення ондансетрону в дозі 8 мг двічі на день вагітній у терміні 14 тижнів після 6 тижнів безуспішного лікування з перервами прометазином, прохлорперазином, метоклопрамідом, внутрішньовенною гідратацією. Ондансетрон контролював блювоту, але не нудоту. Через 2 дні жінку перевели на пероральний прийом препарату в дозі 4 мг 1-2 рази на день до 33 тижня вагітності. Нудота тривала до кінця вагітності, блювота – періодично. Жінка народила здорового хлопчика вагою 2,7 кг на 39 тижні вагітності.
Застосування препарату під час вигодовування:
Застосування ондансетрону матерям, які годують груддю після пологів недостатньо вивчено, але препарат призначений для застосування немовлятам віком від 1 місяця. Комп’ютерна модель продемонструвала, що кількість медикаменту в грудному молоці нижча за клінічну дозу.
Вплив на фертильність (чоловіків та жінок):
Згідно з інструкцією до препарату тестування у щурів при дозах, які у 3,8 разів перевищували рекомендовану для людини внутрішньовенну дозу – 15 мг/кг/день перорально не призводило до порушень фертильності. Відсутня інформація про вплив на фертильність у людини.
Адаптовано за матеріалами:
- Інформаційна система Центру репродуктивної токсикології “Reprotox”.
- Briggs G, Freeman R, Towers C, Forinash A. Drugs in Pregnancy and Lactation: a Reference Guide to Fetal and Neonatal Risk. 12th edition, 2022, Wolters Kluwer. 1461 pages. ISBN: 978-1975-1-6237-5.
- Сайт “MotherToBaby – a service of the Organization of Teratology Information Specialists (OTIS)” (http://www.mothertobaby.org/).
- https://www.drugs.com/pregnancy/ondansetron.html. Інформація з бази даних “Drugs.com”.
- Інформаційна система “Teratogen Information System (TERIS)”.
- https://www.ncbi.nlm.nih.gov/books/NBK500798/. База даних “Drugs and Lactation Database (LactMed)”.
- https://www.webmd.com/baby/what-to-know-about-taking-zofran-for-morning-sickness. Інформація з сайту WebMD.
- https://www.rxlist.com/ondansetron-hydrochloride-drug.htm#warnings. Інформація з бази даних “RxList” мережі WebMD.
Адаптовано 30.03.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних наук, доцент факультетської терапії Ужгородського національного університету.
Переглянуто редакційною колегією 07.05.2023 р.
ЛЕВАЛБУТЕРОЛ
Група/призначення:
Бета-адреноміметики (син. бета-адреностимулятори, бета-агоністи, β-адреностимулятори) для лікування бронхіальної астми. Це R-енантіомер* (право-обертаючий енантіомер) сальбутамолу (албутеролу).
|
*Енантіомери — це стереоізомери, які є неідентичними повними дзеркальними відображеннями один одного (як права і ліва рука). |
Альтернативні назви / синоніми: ксопенекс, левосальбутамол.
Діюча речовина: левалбутамол.
Рекомендації при вагітності:
Відсутні дані про застосування у людини; ймовірно сумісний.
Рекомендації при лактації:
Відсутні дані про застосування у людини; ймовірно сумісний.
Прийом під час вагітності (короткий висновок):
Відсутній досвід застосування у людини при вагітності. Оскільки сальбутамол (албутерол) вважається сумісним з вагітністю, немає підстав не вважати левалбутерол також сумісним.
Інформація щодо досліджень на тваринах:
Репродуктивні дослідження проводились у кролів з дозами, які у 110 разів перевищували добову інгаляційну для людини. Ці дози не були тератогенними. Однак, сальбутамол (албутерол) виявився тератогенним для мишей та кролів.
Інформація щодо впливу на плід:
Відсутній досвід застосування у людини.
Невідомо, чи левалбутерол проникає до плаценти, але його молекулярна вага це припускає. Однак, концентрація в плазмі після інгаляційного застосування є низькою.
Застосування препарату під час вигодовування:
Відсутній досвід застосування у людини. Молекулярна вага левалбутеролу припускає проникнення до грудного молока. Однак, концентрація в плазмі після інгаляційного застосування є низькою. Вплив на плід невідомий, але препарат, ймовірно, є сумісним з грудним вигодовуванням.
Вплив на фертильність (чоловіків та жінок): відсутність інформації.
Адаптовано за матеріалами:
- Інформаційна система Центру репродуктивної токсикології “Reprotox” (http://www.reprotox.org).
- Briggs G, Freeman R, Yaffe S. Drugs in Pregnancy and Lactation: a Reference Guide to Fetal and Neonatal Risk. Ninth edition, 2011, Wolters Kluwer, Lippincott Williams & Wilkins. 1728 pages. ISBN: 978-1-60831-708-0.
Адаптовано 30.03.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних наук, доцент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Переглянуто редакційною колегією 26.04.2016 р.
ЦУКРОВИЙ ДІАБЕТ ТА ВАГІТНІСТЬ
Цукровий діабет (ЦД) – це порушення обміну речовин, при якому не відбувається нормального засвоєння клітинами організму цукру (глюкози) з крові. Абсолютна відсутність інсуліну буває при І типі ЦД. При ІІ типі ЦД інсулін є, його може бути більше, ніж потрібно, але він не працює.
Цукровий діабет під час вагітності (короткий висновок):
Дослідження продемонстрували, що жінки з добре контрольованим діабетом перед вагітністю та низьким рівнем глюкози під час вагітності не мають підвищеного ризику народження дитини з вродженими дефектами.
Високі рівні глюкози під час вагітності збільшують ймовірність народження дитини з вродженими вадами, особливо якщо такий вплив відбувається на плід на ранніх стадіях вагітності, можливо, навіть, поки жінка ще не знає про вагітність.
За деякими оцінками діти матерів з цукровим діабетом в 2-10 разів частіше мають вроджені вади розвитку, найчастіші з яких залучають скелетну, кардіоваскулярну та центральну нервову системи, а рідше сечостатеву та шлунково-кишкову системи.
При плануванні вагітності слід підібрати лікування для утримання рівня глюкози в нормальних межах.
Згідно рекомендації британської національної служби охорони здоров’я (NHS) жінкам з цукровим діабетом, І або ІІ типів, діагностованим до вагітності, в період планування вагітності рекомендована вища за звичайну доза фолієвої кислоти – 5 мг щоденно.
Інформація щодо впливу на плід:
При погано контрольованому діабеті ризик народження дитини з вродженими вадами становить 6-10%, якщо діабет не контролюється в І триместрі, то ризик може підвищуватися до 20%.
Вроджені вади розвитку, характерні для дітей матерів з цукровим діабетом:
- Синдром каудальної регресії (відсутність крижової кістки; відсутність поперекових хребців на різних рівнях; поєднані аномалії інших органів та систем – кінцівок, шлунково-кишкового тракту та сечостатевої системи)
- Гіпоплазія стегна та незвичайного обличчя синдром
- Розщілина хребта (спинномозкова кила; spina bifida) з гідроцефалією та інші вади ЦНС
- Аненцефалія
- Кардіоваскулярні вади: транспозиція магістральних судин, дефекти міжшлункової та міжпередсердної перетинок
- Атрезія анусу та прямої кишки
- Вади нирок: агенезія, мультикистоз, подвоєння сечоводу
- Вади шлунково-кишкового тракту: зворотнє розміщення, трахеостравохідна нориця, атрезія кишечника
При погано контрольованому діабеті також зростає ризик самовільного переривання вагітності, мертвонароджень, прееклампсії, багатовіддя, передчасних пологів. Новонароджені мають підвищений ризик дихальних розладів, гіпоглікемії та жовтяниці.
За деякими даними, навіть, якщо при вагітності діабет ретельно контролюється, у 65% дітей таких матерів виникають наступні ускладнення: гіпоглікемія, гіпербілірубінемія, гіпокальціемія, поліцитемія.
У матерів з діабетом більша ймовірність народження дитини з великою вагою (понад 4 кг). В таких випадках рекомендується кесаревий розтин.
Результати одного з клінічних досліджень свідчать, що частота вроджених вад у дітей матерів з діабетом не цілком залежить від контролю глікемії в період органогенезу. Незважаючи на такі висновки, існує загальноприйнята згода, що правильний метаболічний контроль діабету до моменту зачаття та протягом вагітності є найкращим шляхом для отримання сприятливих результатів вагітностей серед жінок з цим захворюванням.
Ускладнення вагітності частіше зустрічаються та є більш загрозливими, якщо у жінки крім діабету присутні гіпертензія та ожиріння.
Вплив лікування на плід.
Для лікування діабету застосовується інсулін тваринний, людський або синтетичний. Дослідження продемонстрували, що лікування інсуліном при вагітності не асоціювалось із зростанням частоти вроджених вад розвитку. Більш того, інсулін є препаратом вибору при вагітності.
Оральні протидіабетичні препарати також не асоціюються з підвищенням частоти вроджених вад розвитку.
Гестаційний діабет.
Це діабет, який діагностується при вагітності, як правило у терміні 24-28 тижнів. Більшість жінок з гестаційним діабетом не мають симптомів, він виявляється при обов’язковому тестуванні вагітних, але деякі вагітні скаржаться на спрагу, часте сечовипускання, втому.
Більшість жінок з гестаційним діабетом можуть контролювати рівень глюкози за допомогою дієти та фізичних вправ, а частина потребує пероральних препаратів чи ін’єкцій інсуліну. В деяких жінок після пологів рівень глюкози в крові повертається до норми, але близько 50% жінок будуть страждати діабетом в майбутньому.
Оскільки гестаційний діабет виникає, як правило, в ІІ триместрі, він не призводить до зростання частоти вроджених вад розвитку. Однак, цей стан пов’язують з народженням дітей з великою вагою. При поганому контролі гестаційного діабету існує підвищена ймовірність гіпоглікемії та дихальних розладів у новонародженого.
Рідше гестаційний діабет виникає в І триместрі і тоді може підвищуватися ризик вроджених вад розвитку у плода, як і при діабеті в цілому.
Цукровий діабет під час вигодовування:
Жінки з цукровим діабетом можуть вигодовувати немовлят, але діабет повинен добре контролюватися. При деяких дослідженнях виявлено, що надмірний рівень глюкози у матері проникає до грудного молока у вигляді цукру і призводить до гіпоглкемії та підвищення апетиту новонароджених.
Діабет може пригнічувати продукцію грудного молока. Інсулін необхідний для виробітку грудного молока, тому цим пояснюється пригнічення продукції молока при цьому захворюванні.
Деякі дослідники припускають, що грудне вигодовування може знижувати ймовірність розвитку діабету та ожиріння в дитини в майбутньому.
При лікуванні діабету в період вигодовування інсулін не проникає до грудного молока у великих кількостях. Він є сумісним з грудним вигодовуванням.
При прийомі жінкою пероральних протидіабетичних препаратів в період лактації слід контролювати немовлят на наявність ознак гіпоглікемії.
У деяких матерів при грудному вигодовуванні знижується потреба в інсуліні. Матері з діабетом І типу часто відчувають зниження рівня цукру після годування дитини.
Вплив на фертильність (чоловіків та жінок):
Однією з найчастіших причин неплідності у жінок вважаються синдром полікистозних яєчників (Polycystic Ovarian Syndrome (PCOS) та дисметаболічний синдром Х (Dysmetabolic Syndrome X), які асоціюються з ожирінням та діабетом.
У чоловіків ураження нервів при діабеті може призводити до ретроградної еякуляції. Іншим ускладненням діабету є еректильна дисфункція.
У 2007 році наведено попередні дані про можливе пошкодження ДНК сперматозоїдів при цукровому діабеті І типу, що, ймовірно, порушує фертильність.
Адаптовано за матеріалами:
- Сайт “MotherToBaby a service of the Organization of Teratology Information Specialists (OTIS)” (http://www.mothertobaby.org/).
- Інформаційна система Центру репродуктивної токсикології “Reprotox” (http://www.reprotox.org).
- Briggs G, Freeman R, Yaffe S. Drugs in Pregnancy and Lactation: a Reference Guide to Fetal and Neonatal Risk. Ninth edition, 2011, Wolters Kluwer, Lippincott Williams & Wilkins. 1728 pages. ISBN: 978-1-60831-708-0.
- Diabetic care services and pharmacy (US MED site). Available at: http://www.diabeticcareservices.com/diabetes-education/diabetes-and-infertility [Accessed 21 Mar 2016].
- Diabetes and pregnancy. National Health Service of UK (NHS) website [Accessed 24 Mar 2021].
Адаптовано 21.03.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних наук, доцент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Переглянуто редакційною колегією 26.04.2016 р.
ХВОРОБА, ЯКУ СПРИЧИНЮЄ ВІРУС ЗІКА ТА ВАГІТНІСТЬ
Назва англійською мовою: Zika virus, Zika virus infection, Zika virus and pregnancy.
Синоніми:
Вірус Зіка та вагітність; гарячка Зіка та вагітність, Zika вірус.
| ВІРУС ZIKA Є ВИЗНАНИМ ТЕРАТОГЕНОМ ДЛЯ ЛЮДИНИ |
Хвороба, яку спричинює вірус Зіка під час вагітності (короткий висновок):
Вірус Зіка, зазвичай, викликає грипоподібне захворювання з м’яким перебігом, що може включати в себе лихоманку, головний біль, біль в суглобах і/або біль в м’язах, кон’юнктивіт, іноді висипку на тілі. Симптоми починаються через 3-7 днів після укусу зараженого комара і можуть тривати від кількох днів до тижня. Не кожна інфікована вірусом особа матиме симптоми, а тільки 1 з 5. Жінки можуть передавати вірус своїй дитині під час вагітності. Восени 2015 року повідомили про зростання частоти новонароджених з мікроцефалією та іншими аномаліями головного мозку в Бразилії. Матері цих дітей повідомили, що при вагітності перенесли грипоподібне захворювання, а в деяких з них була висипка. В окремих жінок був позитивний результат на наявність вірусу Зіка. Мікроцефалія – це, зазвичай, рідкісна хвороба. У США, як правило, реєструється від 2 до 12 випадків на 10 тисяч новонароджених. Мікроцефалія є досить поширеною в певних районах Бразилії, де її частота становить 1% від всіх народжень. Міністерство охорони здоров’я Бразилії повідомляє про 5909 випадків мікроцефалії або інших вад нервової системи у новонароджених за період від 22 жовтня 2015 року до 27 лютого 2016 року. Також повідомляється про асоціацію між вірусною інфекцією та водянкою плода і внутріутробною загибеллю плода.
Чому потенційний зв’язок між вірусом Зіка і вродженими дефектами не досліджували раніше?
У районах центральної Африки та Азії, де вірус Зіка був поширеним протягом десятиліть, більшість людей заражається в ранньому віці, тому ризик виникнення первинної інфекції під час вагітності є досить незначним. Дотепер населення Америки не мало контакту з вірусом. Це означає, що більшість жінок під час вагітності вперше стали інфіковані. А це, в свою чергу, підвищує ризик народження дітей з вадами.
Інформація щодо впливу на плід:
Поки невідомо, на якому терміні вагітності інфекція, викликана вірусом Зіка може нанести найбільшої шкоди плоду. Зараження на ранніх термінах вагітності, очевидно, буде більш шкідливим, ніж на більш пізніх. Уже відомо, що деякі типи вірусу можуть бути шкідливими для плода як в І, так і в ІІ триместрах.
Вірус Зіка під час вигодовування:
Поки що немає повідомлень про передачу вірусу Зіка через грудне молоко.
Вплив на фертильність (чоловіків та жінок): відсутня інформація.
Додаткова інформація:
У жовтні 2013 – квітні 2014 років у Французькій Полінезії зареєстрована найбільша епідемія вірусної інфекції, викликаної вірусом Зіка. В цей же період відзначили зростання частоти синдрому Гієна-Барре, що припускає можливу асоціацію між цими двома подіями. Так, 41% пацієнтів з синдромом Гієна-Барре мали IgM або IgG до вірусу Зіка і всі 100% мали нейтралізуючі антитіла проти вірусу Зіка при порівнянні з 56% в контрольній групі. 93% пацієнтів з синдромом Гієна-Барре мали IgM до вірусу Зіка, а 88% перенесли вірусне захворювання в середньому за 6 днів до появи неврологічних симптомів, припускаючи інфекцію, викликану вірусом Зіка.
Стани, асоційовані з інфікуванням вірусом Зіка:
ВРОДЖЕНИЙ СИНДРОМ – ZIKA-ВІРУС СИНДРОМ:
|
| Синдром Гієна-Барре (Guillain-Barré syndrome) – це гостра аутоімунна запальна полірадикулонейропатія, яка проявляється млявими парезами і паралічами, порушеннями чутливості, вегетативними розладами. Так як на сьогодні поліомієліт є майже усуненим у більшості країн світу, то синдром Гієна-Барре залишається на даний час найбільш частою причиною гострого млявого паралічу і являє собою одну з серйозних надзвичайних ситуацій в неврології. Також синдром Гієна-Барре може бути описаний як сукупність клінічних синдромів, що включають гостру запальну полірадикулонейропатію з наявністю слабкості та уповільнення рефлексів. |
Повідомляється про випадки передачі вірусу статевим шляхом.
Кращою формою профілактики є захист від укусів комарів. Вакцини для профілактики або лікування вірусу не існує.
Британська біотехнологічна компанія Oxitec створила генетично модифікованих комарів виду Aedes Aegypti шляхом введення двох генів в їхнє ДНК. Завдяки одному з них, личинки комарів світяться під ультрафіолетовим світлом. За словами науковців, це допоможе ідентифікувати комах, що переносять інфекцію. Інший ген спричиняє смерть всього потомства комара. В Oxitec говорять, що заселення генетично модифікованими комарами заражених територій допоможе зменшити передачу вірусу Зіка більш, ніж на 80%.
Адаптовано за матеріалами:
- Сайт “MotherToBaby a service of the Organization of Teratology Information Specialists (OTIS)” (http://www.mothertobaby.org/).
- Інформація Центрів по контролю і запобіганню захворювань (Centers for Disease Control and Prevention(CDC)): http://www.cdc.gov/media/dpk/2016/dpk-zika-virus.html.
- Інформація Всесвітньої організації здоров’я (World Health Organization (WHO)): http://www.who.int/mediacentre/factsheets/zika/en/.
- Інформація Пан-Американської організації охорони здоров’я (Pan American Health Organization. (PAHO)): http://www.paho.org/hq/index.php?option=com_content&view=article&id=11585&Itemid=41688&lang=en.
- Bazley T. Zika virus facts you need to know. Available at http://www.aljazeera.com/news/2016/01/threat-zika-qa-160131093108840.html [Accessed 3 Feb 2016].
- Cao-Lormeau VM, Blake A, Mons S, Lastère S, Roche C, Vanhomwegen J, Dub T, Baudouin L, Teissier A, Larre P, Vial AL, Decam C, Choumet V, Halstead SK, Willison HJ, Musset L, Manuguerra JC, Despres P, Fournier E, Mallet HP, Musso D, Fontanet A, Neil J, Ghawché F. Guillain-Barré Syndrome outbreak associated with Zika virus infection in French Polynesia: a case-control study. Lancet. 2016 Feb 29. pii: S0140-6736(16)00562-6. doi: 10.1016/S0140-6736(16)00562-6. [Epub ahead of print].
Адаптовано 21.03.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних наук, доцент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Переглянуто редакційною колегією 26.04.2016 р.
ДЕПРЕСІЯ ТА ВАГІТНІСТЬ
Депресія – серйозний психологічний розлад, від якого нерідко страждає не тільки сам хворий, але і його родина. Депресивні розлади можуть виникнути в будь-якому віці, в будь-якій соціальній групі.
Депресія під час вагітності (короткий висновок):
Ймовірність розвитку депресії для жінок протягом життя становить 10-25%. Найвищий ризик існує в репродуктивному віці. У деяких жінок пусковим механізмом розвитку депресії є вагітність, що пов’язують зі зміною гормонального статусу та стресом.
| Два дослідження повідомляють про частоту депресії при вагітності на рівні 7-13% |
Інформація щодо впливу на плід:
Деякі дослідження повідомляють про підвищення частоти самовільного переривання вагітності, передчасних пологів, малої ваги при народженні, народження малих для гестаційного віку дітей у випадку нелікованої при вагітності депресії. Одне дослідження повідомляє про підвищену частоту розвитку прееклампсії у жінок з депресією.
Нелікована депресія може також негативно вплинути на подальший розвиток та поведінку дитини.
Окрім того, припинення лікування депресії загрожує рецидивом. Так, вважається, що ризик рецидиву при вагітності в 5 разів вищий, якщо жінка припинила прийом препаратів для лікування депресії при порівнянні з вагітними, які продовжують лікування. Проте ризик рецидиву залишається в будь-якому випадку.
Депресія при вагітності асоціюється зі зловживанням легальними та нелегальними препаратами. Деякі жінки намагаються таким чином лікувати депресію. Однак, зловживання алкоголем та іншими речовинами і препаратами є більш шкідливим, ніж належне лікування депресії. Вживання алкоголю, навіть в невеликій кількості, та паління, а також прийом наркотиків при вагітності пов’язують з негативними наслідками для вагітної та немовляти. Тому депресію слід лікувати призначеними лікарем медичними препаратами.
Більшість антидепресантів не асоціюється з підвищеним ризиком вроджених вад розвитку. При прийомі антидепресантів в ІІІ триместрі у новонароджених можливі дратівливість, порушення сну, порушення частоти дихання та серцебиття. В більшості випадків ці симптоми спостерігаються протягом кількох днів.
Пренатальний нагляд.
Дослідження продемонстрували, що жінки, які страждають психічними захворюваннями, включаючи депресію, нехтують медичним наглядом при вагітності. В цій групі жінок виявлено вищі показники передчасних пологів і смертності немовлят та породілль.
Післяпологова депресія.
Найсерйознішим наслідком нелікованої депресії при вагітності є ризик виникнення післяпологової депресії. Частота післяпологової депресії в загальній популяції становить 5-15% і є вищою у жінок з депресією при вагітності. Припускається, що післяпологова депресія впливає на здатність доглядати дитину та порушує з’язок матері з дитиною, що може мати негативний вплив на розвиток та поведінку дитини.
Депресія під час вигодовування:
Грудне вигодовування покращує здоров’я як матері, так і дитини. Жінки з депресією протягом вагітності можуть вигодовувати немовлят коротший період часу. Таке раннє припинення грудного вигодовування може призвести до повернення симптомів депресії. Якщо жінка здатна продовжувати грудне вигодовування, то прояви захворювання зменшуються і це може навіть попередити післяпологову депресію. Підтримка жінки на ранніх стадіях грудного вигодовування дозволяє їй годувати дитину довший час і є найкращим вибором як для жінки, так і для дитини.
Вплив на фертильність (чоловіків та жінок):
Можливе виникнення депресії на фоні неможливості завагітніти. У всіх пацієнтів з неплідністю є певні симптоми депресії.
Адаптовано за матеріалами:
- Сайт “MotherToBaby a service of the Organization of Teratology Information Specialists (OTIS)” (http://www.mothertobaby.org/).
- Інформаційна система Центру репродуктивної токсикології “Reprotox” (http://www.reprotox.org).
- Briggs G, Freeman R, Yaffe S. Drugs in Pregnancy and Lactation: a Reference Guide to Fetal and Neonatal Risk. Ninth edition, 2011, Wolters Kluwer, Lippincott Williams & Wilkins. 1728 pages. ISBN: 978-1-60831-708-0.
Адаптовано 21.03.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних наук, доцент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Переглянуто редакційною колегією 26.04.2016 р.
ВАКЦИНА ПРОТИ ХОЛЕРИ
Група/призначення:
Вакцина. Покази: профілактика холери.
Альтернативні назви / синоніми: немає.
Діюча речовина: інактивовані бактерії.
Рекомендації при вагітності: сумісна.
Рекомендації при лактації: сумісна.
Прийом під час вагітності (короткий висновок):
Холера при вагітності значно підвищує смертність та захворюваність матері та плода, особливо в ІІІ триместрі. Ризик для плода у випадку вакцинації при вагітності невідомий.
Американська колегія акушерів та гінекологів вважає, що покази до введення вакцини не змінюються з вагітністю.
Інформація щодо досліджень на тваринах: відсутні.
Інформація щодо впливу на плід:
Відсутній досвід застосування.
Застосування препарату під час вигодовування:
Вакцинація при лактації призводить до зростання титру антитіл IgA в грудному молоці, хоча попередні дослідження припускають, що рівень антитіл, індукованих вакцинацією, занадто низький для забезпечення імунітету для немовляти. Повідомляється про вакцинацію 6 жінок в період лактації і значного підвищення у 5 з них титру IgA.
Незважаючи на це, вакцинація матері може захистити немовля від клінічно важкої холери шляхом попередження прямого інфікування дитини від матері.
Вплив на фертильність (чоловіків та жінок): відсутня інформація.
Адаптовано за матеріалами:
- Інформаційна система Центру репродуктивної токсикології “Reprotox” (http://www.reprotox.org).
- Briggs G, Freeman R, Yaffe S. Drugs in Pregnancy and Lactation: a Reference Guide to Fetal and Neonatal Risk. Ninth edition, 2011, Wolters Kluwer, Lippincott Williams & Wilkins. 1728 pages. ISBN: 978-1-60831-708-0.
Адаптовано 04.04.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних наук, доцент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Переглянуто редакційною колегією 26.04.2016 р.
ВАКЦИНА ПРОТИ МЕНІНГОКОКОВОЇ ІНФЕКЦІЇ
Група/призначення:
Вакцина. Покази: профілактика менінгококової інфекції.
Альтернативні назви / синоніми:
Полісахаридна менінгококова вакцина А, С, Y; меномун, менактра.
Доступні наступні формули: 1) полісахаридна менінгококова вакцина групи А, С, Y; 2) комбінована W-135 (меномун A/C/Y/W-135); менактра – штами Neisseria meningitidis серогруп А, С, Y та W-135, білок-носій дифтерійний анатоксин.
Діюча речовина:
Препарат являє собою ліофілізовану суху речовину.
Рекомендації при вагітності: сумісна.
Рекомендації при лактації:
Відсутня інформація про використання у людини; ймовірно сумісна.
Прийом під час вагітності (короткий висновок):
Ризик від вакцинації при вагітності невідомий. При одному дослідженні при вакцинації зареєстрували трансфер до плода материнських антитіл, але він був нерегулярним і не залежав від титру антитіл в матері та терміну вагітності при проведенні вакцинації.
Інформація щодо досліджень на тваринах:
Не проводились з меномуном. У мишей проводились тератологічні дослідження з менактрою. Доза, яка у 900 разів перевищувала рекомендовану для людини, виходячи з площі поверхні тіла, не впливала на фертильність, показники материнської смертності, виживання плодів, постнатальний розвиток. Один з 234 плодів мав розщілину піднебіння і жодний- в контрольній групі. Це була єдина виявлена аномалія, яка, як вважається, не пов’язана з вакциною.
Інформація щодо впливу на плід:
Дослідження 1998 року аналізувала результати вагітностей 34 жінок, які були вакциновані при вагітності, з них 4 (11,8%) в І триместрі, 17 (50%) в ІІ триместрі, 13 (38,2%) в ІІІ триместрі. Результати вагітностей: 34 одноплідні пологи, середній термін нагляду за дітьми 13,2 місяці (1-24 місяці), 1 випадок вродженої вади розвитку. Вроджена вада діагностована у дитини, мама якої отримала вакцину у терміні 33 тижнів. Це був синдром Чарлі М*, який зустрічається з частотою <0,00002%. Такий симптомокомплекс мав би формуватися на ранніх термінах вагітності, генетична природа його не доведена, як і зв’язок з тератогенезом.
|
*Charlie M syndrome) – рідкісне порушення розвитку, що належить до групи синдромів оромандибулярного гіногенезу кінцівок і включає гіпоглоссію, гіподактилію, глосо-піднебінний анкілоз. Основні аномалії: гіпоплазія нижньої щелепи, синдактилія, ектродактилія, малий рот, розщілина піднебіння, гіподонтія, парез обличчя, також гіпертелоризм. |
Рев’ю 1994 стверджує, що вакцина протипоказана при вагітності. Однак, у 1996 році при дослідженні в групі 75 жінок, які вакциновані в ІІІ триместрі, не виявлено несприятливих наслідків у новонароджених.
Застосування препарату під час вигодовування: відсутня інформація.
Вплив на фертильність (чоловіків та жінок): відсутня інформація.
Адаптовано за матеріалами:
- Briggs G, Freeman R, Yaffe S. Drugs in Pregnancy and Lactation: a Reference Guide to Fetal and Neonatal Risk. Ninth edition, 2011, Wolters Kluwer, Lippincott Williams & Wilkins. 1728 pages. ISBN: 978-1-60831-708-0.
- Сайт “MotherToBaby a service of the Organization of Teratology Information Specialists (OTIS)” (http://www.mothertobaby.org/).
Адаптовано 10.04.2016 р.:
Е.Й. Пацкун, лікар-генетик, кандидат медичних наук, доцент кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Переглянуто редакційною колегією 25.04.2016 р.
КРИТИЧНІ ПЕРІОДИ РОЗВИТКУ ПЛОДУ ТА ЧУТЛИВІСТЬ ДО РІЗНИХ ФАКТОРІВ
Альтернативні назви:
Вплив різних факторів в критичні періоди розвитку плоду. Вплив медикаментів в критичні періоди розвитку плоду. Чутливі періоди розвитку плоду та вплив різних факторів.
Виділяють певні періоди при вагітності (критичні), коли формування органів і систем плоду відбувається особливо інтенсивно і він особливо чутливий до дії зовнішніх чинників, таких як хімічні агенти, в тому числі лікарські препарати, радіація, тощо.
Розрізняють наступні періоди:
Перший критичний період – це перші три місяці вагітності, тобто час, коли відбувається закладання і формування тканин і органів плода. Особливо вразливим зародок є на 5-6-й день після зачаття, коли відбувається прикріплення заплідненого яйця в порожнині матки. У цей період розвитку зародок або переносить вплив шкідливих факторів без негативних наслідків, або гине (закон «все або нічого»). На 3-8 тижнях вагітності відбувається процес формування плаценти, який збігається з етапом поділу клітин майбутніх органів і систем плода (органогенез). Ураження зародка саме в цей період веде до виникнення вроджених вад розвитку. При цьому анатомічні порушення виникають в тих органах, які в момент дії шкідливих факторів активно розвивалися.
Другий критичний період: 15-20-й тиждень вагітності. У цей період відбувається посилений ріст головного мозку. На 20-24 тижнях поряд із подальшим зростанням органів плода відбувається становлення і розвиток найважливіших функціональних систем організму (кровообігу, згортання крові, центральної нервової системи та інших). Пошкодження плода в цей час не призводить до формування вади розвитку, але може зумовити виникнення внутрішньоутробного захворювання.
Третій критичний період: 28-34 тижні вагітності. Шкідливі впливи, зокрема, гострі інфекційні захворювання матері, в цей період можуть призвести до передчасних пологів, народження дітей з малою вагою, слабких і навіть до мертвонародження.
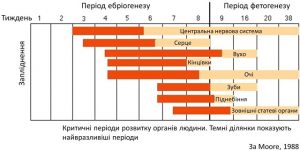
Відомі критичні періоди для кожного органу і системи, що демонструє класична діаграма, створена Moore. Темні смуги на діаграмі демонструють період найбільшої чутливості певного органу до дії шкідливих факторів та ризику основних вроджених вад. Мова йде про великі вроджені вади розвитку. Так, для центральної нервової системи критичним (чутливим) періодом розвитку вроджених вад є 3-5 тижнів, серця – 3,5-6 тижнів, вуха – 4,5-9,5 тижнів, кінцівок – 4,5-7 тижнів, ока – 4,5-8,5 тижнів, зубів – 6-8 тижнів, піднебіння – 6-8 тижнів, зовнішніх геніталій – 7,5-10 тижнів – як видно з діаграми. В основному вади формуються у терміні 3-12 тижнів вагітності. Невеликі і функціональні дефекти нервової системи формуються і на пізніших термінах вагітності.
Питання, які часто можуть виникати при вагітності:
Чи змінюється ризик виникнення певних вроджених вад під час вагітності ?
Так, ризик залежить від того, який орган чи система дитини розвивались в момент впливу медикаменту чи іншого фактору. Якщо орган на цей час вже був сформований, то вада розвитку вже не може виникнути, але можливий вплив на ріст та функцію певного органу.
Який найбільший ризик при впливі чинників на дуже ранніх термінах вагітності?
При впливі на дуже ранньому терміні вагітності існує найвищий ризик самовільного переривання вагітності. Можливий викидень навіть до того, як жінка розуміє, що вона вагітна. На цій ранній стадії клітини ембріону мають велику здатність до відновлення. Якщо викидень не відбувся, то вважається, що формування вроджених вад є малоймовірним.
Перші 4 тижні вагітності називають «все або нічого». «Все» – це важке пошкодження, що призводить до викидня. «Нічого» – вплив, який не дає наслідків.
Який найвищий ризик при впливі протягом І триместру вагітності?
При впливі в І триместрі є високий ризик вроджених вад розвитку.
Який найвищий ризик при впливі у ІІ та ІІІ триместрах?
При впливі в ІІ та ІІІ триместрах виникають проблеми росту і можуть формуватися незначні вроджені вади. При цьому також виникають функціональні порушення в майбутньому, такі як проблеми з навчанням. І, нарешті, застосування певних медичних препаратів в кінці вагітності може призвести до синдрому відміни в деяких новонароджених.
Чи означає це, що вплив може бути шкідливим в певний час під час вагітності, але не в інший час?
Так. Наприклад, якщо жінці призначено препарати, які підвищують ймовірність вад серця, то при прийомі в ІІІ триместрі вади не виникатимуть. Відомо, що критичним періодом формування вад серця є 3 – 6 тижні вагітності. Тому призначення в цей період і може призвести до вроджених вад серця у плода.
Адаптовано за матеріалами:
- Сайт “MotherToBaby a service of the Organization of Teratology Information Specialists (OTIS)” (http://www.mothertobaby.org/).